Gli animali sia selvatici che da reddito esposti ai PFAS possono avere effetti negativi sulla sfera riproduttiva, e rappresentare degli eventi sentinella sia per la valutazione della biodiversità, sia per possibili effetti tossici sul genere umano. Si discuterà di questi aspetti in una giornata ECM organizzata dall’IZS del Mezzogiorno, con la partecipazione del Centro di Riferimento per i PFAS negli alimenti e nei mangimi – IZS dell’Abruzzo e Molise.
Se in campo umano la tossicità riproduttiva dei PFAS non appare ancora così consolidata come per altri effetti, quali quelli sul sistema immunitario, sulla epatotossicità, sulle dislipemie, e non da ultimo per il PFOA per effetti genotossici, ci sono consolidate evidenze che l’esposizione a PFAS in animali selvatici e da reddito ovipari e ovovivipari possa seriamente compromettere la capacità riproduttiva.
Questo può avere conseguenze sia sulla biodiversità, che sulla qualità e quantità delle produzioni alimentari, dalle api, ai pesci, per arrivare alle galline ovaiole.
Il meccanismo di azione tossica è stato identificato nella capacità di alcuni PFAS di legarsi alla vitellogenina, la proteina di trasporto dei lipidi alla cellula uovo. Il complesso vitellogenina – PFAS, interagendo con il recettore specifico della vitellogenina sulla membrana dell’oocita, viene internalizzato. I PFAS endocellulari possono quindi raggiungere il nucleo, e attraverso un meccanismo di tossicità legato allo stress ossidativo, impedire la riparazione delle rotture del DNA, rotture frequenti nelle cellule germinali in attiva fase di moltiplicazione/differenziazione.
La conseguenza tossicologica è la infertilità, anche dovuta ad una morte embrionale precoce.
Tali evidenze sono state recentemente sottolineate da uno studio osservazionale sulla percentuale di schiusa delle uova della tartaruga marina Caretta caretta dai colleghi degli II.ZZ.SS. della Campania e dell’Umbria, in collaborazione con l’Istituto Superiore di sanità e la Stazione Zoologica “Anton Dohrn” di Napoli. Approfittando di un incremento dei siti di nidificazione durante il periodo di lockdown da COVID-19 sulle coste campane, è stata notata una significativa correlazione negativa tra contenuto di PFAS/PFOS nelle uova non schiuse, e la percentuale di schiusa della nidiata, riferita a 41 differenti siti di deposizione.
In maniera interessante, le concentrazioni di PFOS/PFAS determinate sono relativamente ridotte, nell’ordine di pochi ng/g, e largamente riconducibili alla contaminazione basale del Mediterraneo. Solo il numero rilevante di uova deposte (in media 86 per nido) ha permesso di avere la adeguata sensibilità nel verificare tale effetto tossico, difficile da rilevare in animali che depongono poche uova. Probabilmente si è in presenza di uno degli end-points tossicologici più “conservativi” , ovverossia effetti avversi rilevabili a dosi molto basse. Basti pensare che passare da una contaminazione di 1 ng/g PFOS a 3 ng/g PFOS determinerebbe una riduzione di schiusa del 30% .
Il meccanismo di trasferimento dei PFAS alla cellula uovo, esemplificato dagli Autori trova peraltro conferma nel trasferimento della contaminazione descritto in altri lavori relativo a mangimi contaminati con PFAS e le relative uova di gallina.
Di questi aspetti se ne discuterà in una giornata ECM organizzata dall’IZS del Mezzogiorno, con la partecipazione del Centro di Riferimento per i PFAS negli alimenti e nei mangimi – IZS dell’Abruzzo e Molise.
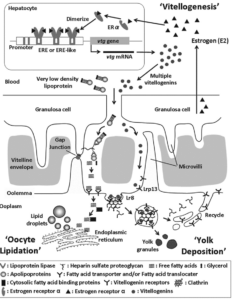
| Schema che illustra il ruolo della vitellogenina, sintetizzata dal fegato sotto fase estrogenica, nel veicolare lipidi e PFAS direttamente all’oocita, tramite specifica interazione con il recettore di membrana. Da Reading et al., doi:10.3390/fishes3040045 |
E negli animali non ovipari e ovovivipari? La vitellogenina in tali animali è ormai un gene non più espresso (pseudogene); tuttavia, è possibile che altre proteine incaricate del trasporto lipidico nel sangue possano avere la stessa funzione di veicolare i PFAS alle cellule germinali femminili. In tale ambito l’ipofertilità potrebbe essere anche legata ad una riduzione del numero di cellule germinali nell’ovaio, per interferenza dei PFAS con la meiosi, in mancanza del tuorlo. Test in animali di laboratorio avvalorano tale ipotesi, che trova una conferma epidemiologica in un recente studio condotto sulla popolazione femminile esposta a PFAS a Singapore.
Tornando alle nostre zone venete “sovraesposte” sarebbe oltremodo interessante associare la presenza di PFAS con effetti ecotossicologici in invertebrati e vertebrati, che riconoscano nella vitellogenina il carrier dei PFAS agli oociti. Che lo stato di sofferenza delle vongole in laguna sia anche legato a tale esposizione? Di certo le azioni di monitoraggio ambientale e alimentare intraprese nella Regione potrebbero beneficiare anche di un approccio ecotossicologico.
IL PROGRAMMA dell’evento “PFAS tra Ambiente e Salute: aspetti analitici e studi di monitoraggio“
| Tabella che illustra gli effetti tossici più consolidati dei PFAS sulla salute umana, tratta dalla proposta di restrizione dei PFAS avanzata in ambito REACH – Allegato XV. In blu scuro, gli effetti su cui è più forte l’associazione con l’esposizione a PFAS. |

Per chi ne volesse sapere di più:
https://doi.org/10.1016/j.envpol.2023.123257
https://doi: 10.1002/vetr.4021



